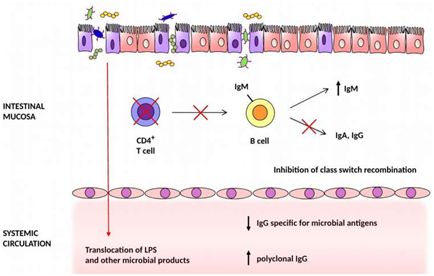
图片来自Zdenek Hel et al., PLoS Pathogens, doi:10.1371/journal.ppat.1006087.
2017年1月31日/生物谷BIOON/---在HIV-1感染的头几周内,肠道与血液之间的物理屏障遭受到严重的破坏。这能够允许肠道中的所有微生物和微小的细菌碎片进入血液,从而促发能够导致获得性免疫缺陷综合征(AIDS, 俗称艾滋病)的炎症,而且即便是这种病毒的复制受到药物治疗的控制,也会如此。
在一项新的研究中,来自美国阿拉巴马大学伯明翰分校的研究人员利用一种新的技术分析了从81名HIV-1感染者和25名对照者肠道内收集的液体中的抗体,结果发现HIV-1感染者具有异常的肠道抗体水平。他们说,这种抗体调节异常可能是导致肠道不能够阻止炎性微生物入侵血液的一种重要因素。相关研究结果于2017年1月26日发表在PLoS Pathogens期刊上,论文标题为“Dysregulation of Systemic and Mucosal Humoral Responses to Microbial and Food Antigens as a Factor Contributing to Microbial Translocation and Chronic Inflammation in HIV-1 Infection”。
在阿拉巴马大学伯明翰分校病理学系副教授Zdenek Hel博士的领导下,研究人员采用了一种被称作蛋白芯片分析的技术。总共有39种不同的肠道细菌蛋白抗原被用来结合肠道洗液中的抗体。多种食物抗原也被用来结合抗体。他们随后能够测试哪些类型的抗体在HIV-1阳性测试者和HIV-1阴性测试者体内产生。
Hel和同事们发现HIV-1感染者和HIV-1未感染者都会产生抵抗这些细菌抗原和食物抗原的抗体。然而,这两组测试者在产生的抗体类型上存在着巨大的差异。
相比于能够更好地结合抗原的抗体类型:IgG和IgA,HIV-1感染者具有更高比例的不那么成熟的抗体类型:IgM。这提示着肠道内层(即粘膜)中的免疫系统细胞不能够制造阻止细菌碎片进入血液所需的这些抗体类型。
再者,研究人员说,IgM在肠道粘膜中积累可能形成加剧炎症的免疫复合物。
众所周知,在具有健康的免疫系统的人体内,抗体产生细胞会从早期的IgM产生切换到后期的IgG和IgA产生。人们也很好地了解到HIV-1感染会导致肠道粘膜中的免疫记忆细胞较早地和显著地耗竭,而这些细胞是进行抗体类型切换所必不可少的。
Hel和同事们关于 HIV-1感染与显著上升的IgM水平和下降的IgG/IgM和IgA/IgM比例相关联的发现与这些肠道粘膜记忆性CD4+ T细胞丢失是相一致的。
Hel说,“这项研究涉及相对较小数量的病人,而且并不包括对肠道细胞进行直接分析。不过,这些发现能够改善我们对HIV-1如何破坏免疫系统的理解,从而为开发潜在的新疗法提供信息。”(生物谷 Bioon.com)
本文系生物谷原创编译整理,欢迎转载!点击 获取授权 。更多资讯请下载生物谷app。
Dysregulation of Systemic and Mucosal Humoral Responses to Microbial and Food Antigens as a Factor Contributing to Microbial Translocation and Chronic Inflammation in HIV-1 Infection
Zdenek Hel , Jun Xu, Warren L. Denning, E. Scott Helton, Richard P. H. Huijbregts, Sonya L. Heath, E. Turner Overton, Benjamin S. Christmann, Charles O. Elson, Paul A. Goepfert, Jiri Mestecky
doi:10.1371/journal.ppat.1006087
尊敬的 先生/女士
您已注册成功,注册信息及注意事项已发到联系人及参会人邮箱,请注意查收。如未收到,请联系大会联系人。