肺癌是最常见的癌症之一(占总病例的11.4%),仍然是癌症死亡的主要原因(占总癌症死亡的18.0%),其中肺腺癌(LUAD)占大多数。目前,手术结合围手术期化疗或放射治疗仍然是肺部恶性肿瘤的标准治疗方法。
根据国家癌症综合网络(NCCN)指南(v3.2021)的建议,以铂类化合物为基础的联合化疗,如顺铂(CDDP)和培美曲塞(PEM),几十年来一直是LUAD最活跃的一线治疗方案。然而,在LUAD患者中,CDDP/PEM的抗肿瘤效果往往受到固有或获得性多药耐药(MDR)的限制,从而导致治疗失败和预后不良。
尽管在肿瘤细胞调控药物外排、DNA损伤修复、细胞周期和细胞凋亡以及影响细胞命运的信号通路等方面进行了广泛的研究,但可能驱动CDDP/PEM多药耐药的关键因素和机制仍然不清楚。

图片来源: https://doi.org/10.1016/j.omtn.2022.03.020.
近日,来自复旦大学的研究者们在Molecular Therapy: Nucleic Acids杂志上发表了题为“miR-6077 promotes cisplatin/pemetrexed resistance in lung adenocarcinoma via CDKN1A/ cell cycle arrest and KEAP1/ferroptosis pathways”的文章,该研究结果表明miR-6077在LUAD对CDDP/PEM的敏感性中发挥了关键作用,从而为临床克服化疗耐药提供了一种新的治疗策略。
肺腺癌(LUAD)是世界上最常见的恶性肿瘤之一。顺铂(CDDP)加培美曲塞(PEM)联合化疗仍然是主要的治疗方案,但化疗耐药性极大地限制了其治疗潜力。在这里,通过CRISPR-Cas9筛选,研究者确定miR-6077是LUAD中CDDP/PEM耐药的关键驱动因素。
功能实验证实,在细胞系和患者来源的异种移植模型中,异位过表达miR-6077使LUAD细胞对CDDP/PEM减敏。通过细胞内RNA测序和CDDP/PEM治疗患者样本的单细胞测序,研究者观察到CDDP/PEM诱导CDKN1A和Keap1上调,进而分别激活细胞周期停滞和铁死亡,从而导致细胞死亡。通过miRNA下拉实验,研究者确定并验证了miR-6077靶向CDKN1A和Keap1。
此外,研究者还证明miR-6077通过CDKN1A-CDK1介导的细胞周期停滞和Keap1-NRF2-SLC7A11/NQO1介导的铁死亡来保护LUAD细胞免受CDDP/PEM诱导的细胞死亡,从而导致体内和体外多个LUAD细胞产生化疗耐药。此外,研究者还发现GMDS-AS1和LINC01128通过海绵化miR-6077使LUAD细胞对CDDP/PEM增敏。
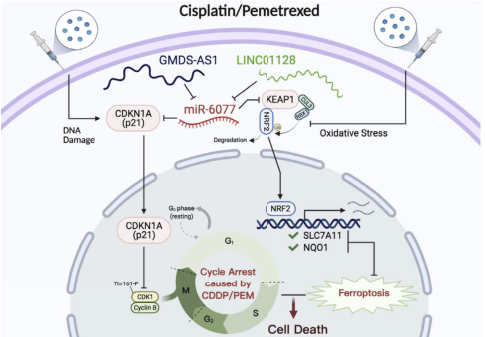
机制示意图
图片来源: https://doi.org/10.1016/j.omtn.2022.03.020
总之,这项研究提供了首次报道的全面证据,表明miR-6077导致了对CDDP/PEM的耐药性,是接受联合化疗的LUAD患者的预后生物标志物。研究者阐明了CDKN1A和Keap1的特异性靶向是miR-6077减轻CDDP/PEM诱导的G2/M期停滞和铁死亡的分子机制。
此外,GMDS-AS1和LINC01128作为miRNA海绵发挥作用,从而在调节LUAD化疗耐药方面产生与miR-6077相反的作用。因此,这些发现对于我们理解LUAD多药耐药的发展具有重要意义,靶向上述不同的分子可能为LUAD对CDDP/PEM治疗不敏感提供新的治疗策略。(生物谷 Bioon.com)
http://meeting.bioon.com/2021Gene
尊敬的 先生/女士
您已注册成功,注册信息及注意事项已发到联系人及参会人邮箱,请注意查收。如未收到,请联系大会联系人。